Amr Elboushia , Mohamed Elsherbenia , Abdelrahman M. Gameela, Waleed Soroura , Mohamed Aminb , A. Samira , A. Salema
Article in The Egyptian Journal of Surgery · January 2019
DOI: 10.4103/ejs.ejs_150_18
介 绍
静脉内消融已被用于治疗静脉曲张和已成为治疗轴向反流的首选技术之一。最初推荐直径小于8 毫米,之后外科医生逐渐掌握治疗较大静脉的经验。对于较粗大的静脉治疗一直存在争议,一些外科医生建议手术治疗,而另一些则建议静脉内消融。
患者和方法
根据患者的大隐静脉直径,和3个月、6个月和12个月的双相随访时间分为三组。采用目测类比评分法分别评估术后第1周和第4周的疼痛。
结 果
在我们的研究中,没有任何一组病人发生深静脉血栓形成 (DVT) 或神经损伤。1周时,两组间差异有统计学意义;但4周时术后疼痛差异无统计学意义。在3个月双相扫描中均无再通,闭塞率为100%。在6个月和12个月时,两组间的再通无显著性统计学差异。
结 论
我们的研究表明,腔内激光消融术在治疗粗大直径大隐静脉的短期效果良好。腔内激光的使用必须是一个动态过程,作为血管外科医生。可以通过改变各种参数以优化激光的最终手术效果。
关键词
静脉内激光治疗,大直径大隐静脉,线性静脉内能量密度,静脉曲张
慢性静脉功能不全,是自人类文明诞生以来一直存在的公共健康问题之一,一直造成经济和社会负担[1,2]。大概四分之三的病例由大隐静脉(GSV)病变引起静脉曲张症状[3]。
目前静脉内消融治疗静脉曲张已被广泛用于治疗静脉曲张,并作为治疗轴向反流的首选技术之一,逐渐受到血管外科医生的欢迎。最初推荐的直径小于8mm,之后外科医生逐渐掌握治疗粗大静脉的经验。粗大静脉的治疗一直存在争议,一些外科医生建议手术,而其他医生建议静脉内消融[4-6]。使用静脉内激光治疗(EVLA)的目的是通过静脉阻塞来阻止逆行血流。这是通过热损伤导致血管内膜和中膜破坏,引起静脉壁纤维化和静脉非血栓性阻塞[7]。
使用EVLA已经显示了良好的长期结果[8],2013年的NICE指南推荐EVLA用于轴向静脉曲张反流的首选方式之一,该指南于2016年2月获得批准和更新[9]。
臻岱环激光波长是被水吸收的波长之一,环形的光纤设计有利于将能量均匀地扩散到静脉壁,静脉壁穿孔的发生率较小[10]。臻岱环激光手术系统显示了良好的闭塞效果,复发率约为2-5%[11]。
线性静脉内能量密度(LEED),已被大多数操作者用作一种测量激光能量输送到静脉导致闭塞的方法。LEED越高,传递的能量越多,静脉壁破坏越严重,并与并发症和疼痛风险增加相关。
本研究的目的是比较高能EVLA治疗粗大直径静脉曲张的有效性和安全性[12]。
患者和方法
病 人
本研究纳入的患者,从2015年2月至2017年6月接受我中心5名血管外科医生的治疗。所有患者在门诊记录身高和体重,计算其BMI值。本研究纳入了糖尿病控制、高血压控制的患者,排除未控制糖尿病、高血压,周围血管疾病、既往干预后复发、小隐静脉反流、活动性感染、静脉溃疡的患者。经过我们团队的双相检查,将患者分为三组:第一组为GSV节段最高可达12mm的肢体;第二组为GSV节段13-20mm的肢体,第三组为GSV节段大于20mm的肢体。所有测量都是在站立位下进行。干预的所有步骤,包括麻醉的类型和可能获得的并发症,都与所有患者仔细讨论,并获得所有患者的书面同意。
过 程
使用设备为臻岱环激光手术系统和尖端360°环形光纤。
术前确认回流大于500ms后,在站立位用双超声(US)测量GSV。在皮肤上标记GSV每个节段直径。所有患者的手术均在脊髓麻醉下进行。采用超声引导下改良Seldinger技术,在腿上三分之一处GSV穿刺,如果静脉弯曲明显,则在较高的水平穿刺第二或第三鞘。导入激光光纤,其尖端位于距隐股交界处1.5cm。患者的体位改为头低脚高,将肿胀液注射到静脉周围进入隐室。
需要注意肿胀液的注射量,用于包裹在GSV和大腿上部到股骨沟的血管周围,特别是超过12mm的静脉,以形成一道1.5-2cm左右吸收热量的保护层。在不超过12mm的静脉中,由肿胀液产生的吸热范围为1-1.5cm左右即可。对于直径超过12mm的静脉,可以使用冷却生理盐水来增加吸热的效果。
在我们的研究中,使用了连续和脉冲两种激光发射模式。脉冲模式为每次脉冲发射1s,间隔0.5s。在开始激光发射之前,使用超声探头定位隐股交界处,通过压迫以减少热能进入股静脉的风险。
对大于12mm的静脉,激光功率调整为10W,回拉光纤。根据光纤传导的静脉壁收缩感,和超声监视下静脉的闭塞程度,减慢或加快回拉速度。Dabbs等人[12]所描述的不均匀收缩的大静脉,采用多通道穿刺,直至完全闭塞。
记录治疗后的GSV的长度、每个节段激光发射的能量以及术中双相检查结果。当治疗段无血流时,手术成功。
我们的最终记录是12个月时血管闭塞有效性。1周后安排了常规双相扫描,以排除深静脉血栓形成(DVT)。在术后第1周和第4周,通过目测类比评分法对术后疼痛进行评估。评分的范围从0(没有疼痛)和100(更严重的疼痛)。患者分别在3个月、6个月和12个月时进行双相检查评估。排除未参加任何评估的患者,第1组、第2组和第3组分别排除7名、4名和2名患者。
统计分析
数据采用SPSS statistics 23(SPSS Corp., Armonk, New York, USA)进行分析。如果P值小于0.05,则认为差异有统计学意义。分类变量比较采用费希尔精确检验3×2列联表,数值数据的比较采用方差分析和事后分析,以便需要时进行组内分析。
结 果
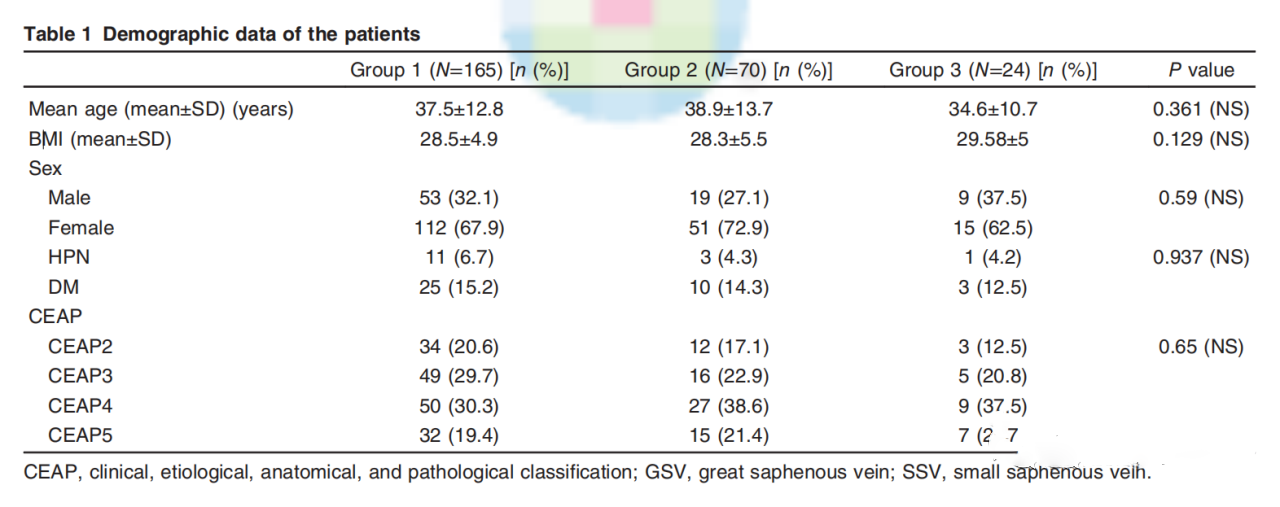
我们的研究包括185名患者的259条下肢。统计数据如表1所示。组间性别、平均年龄、BMI、共病或临床、病因、解剖和病理分类均无显著统计学差异(P> .5)。
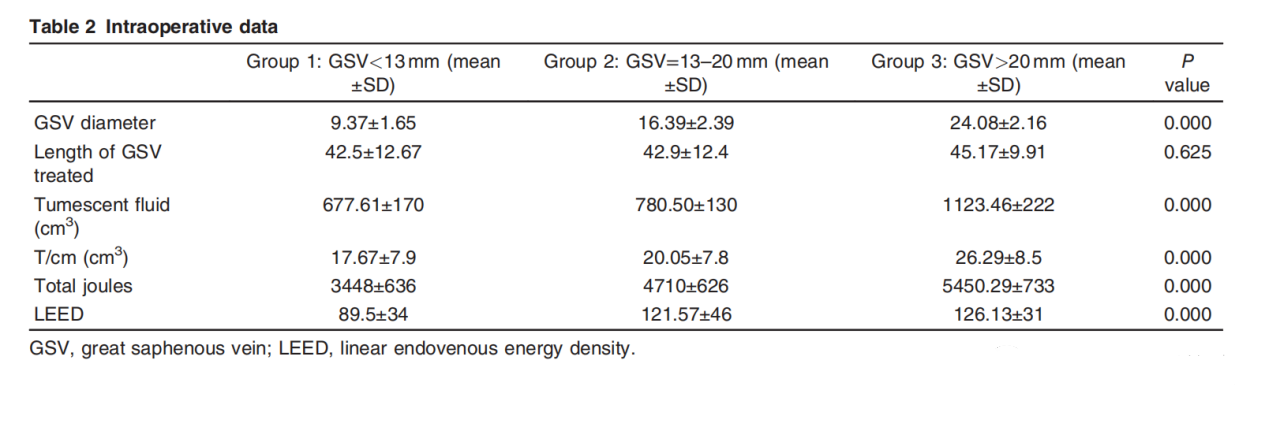
组间在术中数据方面存在显著差异:因为肿胀液量平均值、每厘米肿胀液、总焦耳和每厘米焦耳数都有差异,反映了更高能量的使用,用于压缩静脉的肿胀液起到了吸收热量的作用。组间静脉治疗长度差异无统计学意义。该数据如表2所示。
术后发现
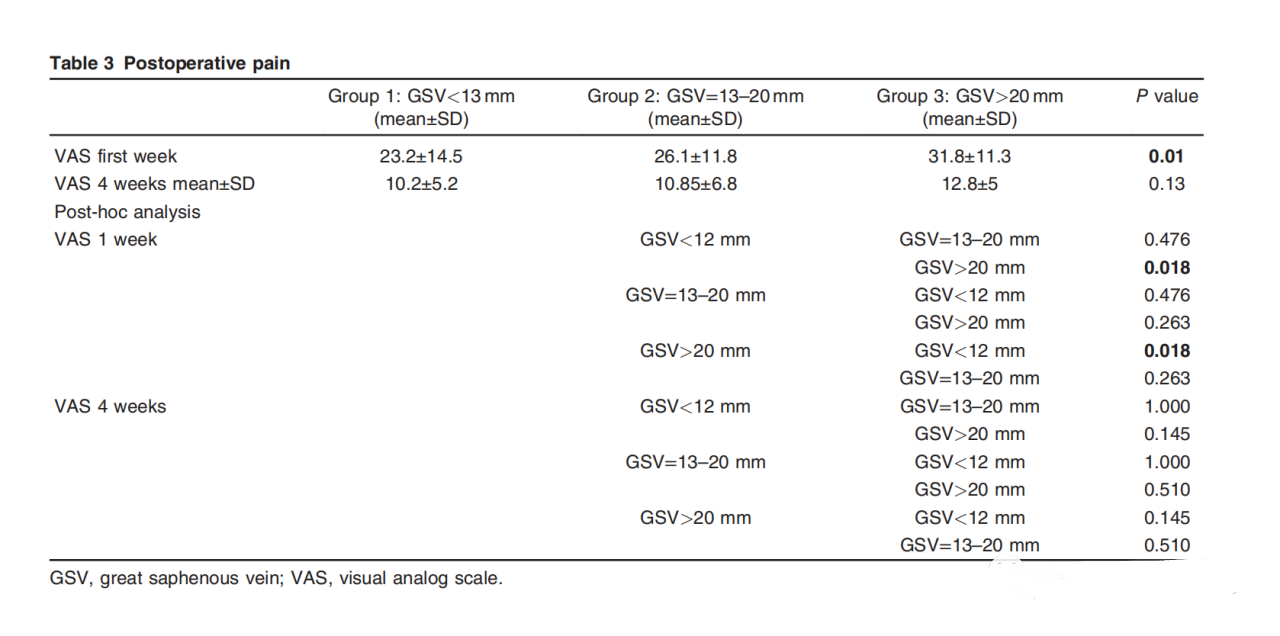
在我们的研究中,没有发生深静脉血栓、烧伤或永久性感觉异常。术后疼痛采用目测类比评分法进行评估。第1周时,两组间有显著差异,第4周时无显著差异。采用事后分析进行组内分析,术后第一周VAS评分中,组1和组3的疼痛差异有统计学意义(表3)。
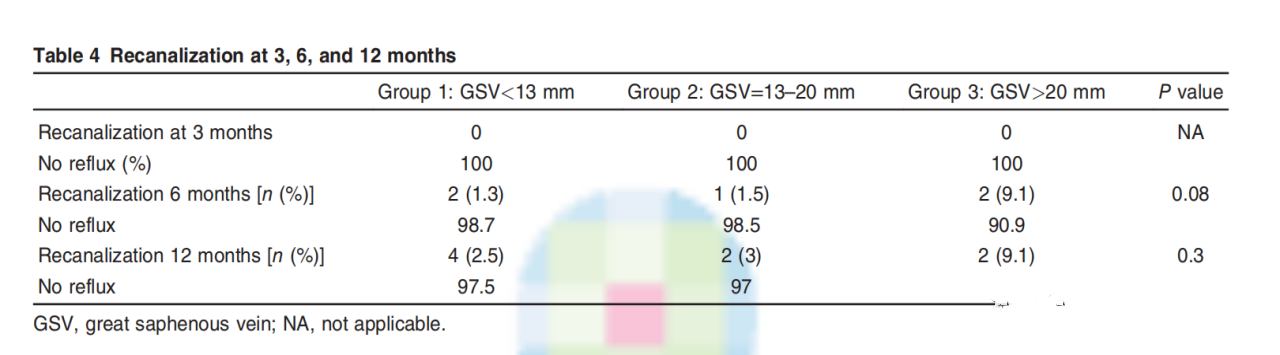
所有组在3个月双相扫描中均未出现术后再通,闭塞率为100%。
在6个月时,第一组的再通率为1.3%(2例),而第二组为1.5%(1例),第三组为9.1%(2例)。组间无显著性差异。
在12个月时,第一组的再通总数为2.5%(4例),第二组为3%(2例),第三组为9.1%(2例)。这些数据并没有显示组之间在再通方面有任何显著的统计学差异(表4)。
讨 论
减少EVLA复发的关键因素是了解复发的机制,设计出减少复发的最佳策略。
一些研究表明,与开放手术相比,EVLTA在治疗直径超过8mm的曲张静脉时效果不好,这是由于对静脉的不完全消融导致血栓形成,引起深静脉血栓的风险加大或成为细胞培养基导致细胞迁移引起血管再通[4-6,13,14]。这不是我们研究的结论,但我们与其他建议使用EVLA治疗更大的隐静脉直径[12,15]的研究中,关于闭塞和再通的结果相似。
多项研究证实:静脉壁热损伤程度越小,再通的风险越大[6,16]。我们同意Dabbsetal.[12]透壁静脉壁损毁是EVLA治疗静脉曲张的关键,因为它会导致血管纤维化闭塞。而静脉内壁未受到激光热能充分灼烧的部分,形成血栓性静脉炎,是一种良好的培养基,细胞从中迁移引起静脉再通导致复发。
Cowpland等人[17]在2016年发表的一篇非常有趣的文章中,回顾了影响最佳LEED的临床证据,并确定了影响最佳LEED的不同因素,包括静脉直径、光纤设计、激光波长、光纤回撤率和激光传递方式。
在扩张程度大的静脉内,仅仅增加LEED量,不足以充分破坏静脉内壁造成热损伤,这就是为什么我们要在超声引导下对静脉未闭塞的部分进行多通道穿刺(Dabbs等人在他们的研究中描述了这项技术),确保其纤维化非血栓性闭塞,降低复发风险。这也得益于足够数量的肿胀液体来充分压迫静脉,和适当的头低脚高位排空静脉。
光纤尖端的设计是另一个重要的因素。环形光纤将激光能量360°均匀分布,以极低的热能损毁静脉壁。其中双环光纤[11]和锥形光纤[18]也可以通过较低的LEED,得到满意的闭塞率。
另一个影响治疗结果的因素,是虽然使用了固定的光纤回拉率,但没有感觉到静脉壁的挛缩,也没在超声下观察到闭塞。光纤的回拉可以通过加快或放慢回拉率,从而增加或减少热量损伤的传递,无需使用最大的激光能量。Ignatieva等人[19]在2017年发表的一项实验研究中也强调了这一点,该研究表明,光纤回退率和激光功率决定了消融温度与胶原组织的损毁程度。在我们的研究中,我们没有使用脉冲模式和连续模式进行比较,但我们确实注意到光纤的尖端几乎没有碳化痕迹。一些研究证实,与连续或不连续的模式相比,脉冲波模式能提供足够的能量,而不会导致过度的组织碳化或静脉壁穿孔[20,21]。
在多项研究中,针对水吸收的激光波长(1320、1470和1510nm)与较短波长(针对血红蛋白为吸收介质,810、980nm)相比,具有更好的闭合率,平均LEED值更低[22-25]。静脉直径大于20mm组的术后疼痛最初显著,但一个月后疼痛消失,没有异常感觉。
把不同激光波长的EVLA技术放在一起对比,从而得出结论认为激光腔内消融不适合较大直径静脉曲张的治疗,对于患者和不断发展的激光技术而言显然是不公平的。我们鼓励在轴向静脉曲张治疗中优先选择腔内消融,调节不同的治疗参数是一个动态过程,从而适应不同的病例治疗。
我们的研究有局限性,是一项非随机的短期研究,由5名血管外科医生做EVLA术,未设开放手术组作为较大直径静脉的对照组。需要进一步的随机对照试验和长期研究来证实EVLA在较大扩张的静脉曲张中的优势[26]。
结 论
本研究显示EVLA治疗较大直径GSV具有良好的短期效果。采用适当的LEED值和多通道穿刺技术是改善静脉闭塞和诱导静脉壁纤维化的好方法。EVLA的使用必须是一个参数动态组合的过程,作为一名血管外科医生,你可以改变各种参数,如激光能量、光纤回撤速度、多次灼烧和注射的膨胀液量,以优化手术的最终结果。这可能会改变我们认为EVLA不适合治疗大于12mm的静脉曲张的观点。
参考文献:
1,Wittens C, Davies AH, Bækgaard N, Broholm R, Cavezzi A, Chastanet S, et al. Editor’s choice E management of chronic venous disease: clinical practice guidelines of the European society for vascular surgery (ESVS). Eur J Vasc Endovasc Surg 2015; 49:678e737.
2,Carpentier PH, Maricq HR, Biro C, Ponçot-Makinen CO, Franco A. Prevalence, risk factors and clinical patterns of chronic venous disorders of lower limbs: a population-based study in France. J Vasc Surg 2004; 40:650e9.
3,Munasinghe A, Smith C, Kianifard B, Price BA, Holdstock JM, Whiteley MS. Strip-track revascularisation after stripping of the great saphenous vein. Br J Surg 2007; 94:840–843.
4,MacKenzie RK, Cassar K, Brittenden J, Bachoo P. Introducing endovenous laser therapy ablation to a national health service vascular surgical unit − the Aberdeen experience. Eur J Vasc Endovasc Surg 2009; 38:208–212.
5,Starodubtsev V, Lukyanenko M, Karpenko A, Ignatenko P. Endovenous laser ablation in patients with wide diameter of the proximal segment of the great saphenous vein: comparison of methods. Phlebology 2014; 30:700–705.
6,Fernandez CF, Roizental M, Carvallo J. Combined endovenous laser therapy and microphlebectomy in the treatment of varicose veins: efficacy and complications of a large single-center experience. J Vasc Surg 2008; 48:947–952
7,Min RJ, Khilnani N, Zimmet SE. Endovenous laser treatment of saphenous vein reflux: long-term results. J Vasc Interv Radiol 2003; 14:991–996.
8,Ravi R, Trayler EA, Barrett DA, Diethrich EB. Endovenous thermal ablation of superficial venous insufficiency of the lower extremity: single-center experience with 3000 limbs treated in a 7-year period. J Endovasc Ther 2009; 16:500–505. doi: 10.1583/09-2750.1.
9,National Institute for Health and Care Excellence. Varicose veins in the legs: the diagnosis and management of varicose veins. London: National Institute for Healthand Care Excellence. 2013. Available at:
http://publications.nice.org.uk/varicose-veins-in-the-legs-cg168. [Accessed 1August 2018].
10,Lawson J, Gauw SA, Vlijmen CJV, Pronk P, Gaastra MTW, Tangelder MJ,et al. Prospective comparative cohort study evaluating incompetent great saphenous vein closure using radiofrequency-powered segmental ablation or 1470-nm endovenous laser ablation with radial-tip fibers (Varico 2 study). J Vasc Surg Venous Lymphat Disord 2018; 6:31–40.
11,Shaidakov EV, Grigorian A, Bulatov V, Porembskaya O,Rosukhovsky D. Results of great saphenous vein endovenouslaser ablation with a wavelength of 1470 nm using radial 2ring fiber with different linear energy density. J Vasc Surg Venous Lymphat Disord 2017; 5:151.
12,Dabbs EB, Mainsiouw LE, Holdstock JM, et al. A description of the ‘smile sign’ and multi-pass technique for endovenous laser ablation of large diameter great saphenous veins. Phlebology 2017;0:1–612.
13,Gloviczki P, Comerota AJ, Michael C, et al. The care of patients with varicose veins and associated chronic venous diseases: clinical practice guidelines of the Society for Vascular Surgery and the American Venous Forum. J Vasc Surg 2011; 53:2–48.
14, Atasoy M. Efficacy and safety of endovenous laser ablation in very large and tortuous great saphenous veins. J Vasc Interv Radiol 2015; 26:1347–1352.
15,Starodubtsev V, Lukyanenko M, Karpenko A, et al. Endovenous laser ablation in patients with severe primary chronic venous insufficiency. Int Angiol 2017; 36:368–374.
16,Corcos L, Dini S, Anna D, et al. The immediate effects of endovenous diode 808-nm laser in the greater saphenous vein: morphologic study and clinical implications. J Vasc Surg 2005; 41:1018–1024.
17,Cowpland C, Cleese A, Whiteley M. Factors affecting optimal linear endovenous energy density for endovenous laser ablation in incompetent lower limb truncal veins − a review of the clinical evidence. Phlebology 2016; 32:299–306.
18,Cavallini A, Marcer D, Ferrari Ruffino S. Endovenous ablation of incompetent saphenous veins with a new 1,540-nanometer diode laser and ball-tipped fiber. Ann Vasc Surg 2014; 28:686–694.
19 Ignatieva N, Zakharkina O, Masayshvili C, et al. The role of laser power and pullback velocity in the endovenous laser ablation efficacy: an experime study. Lasers Med Sci 2017; 32:1105–1110.
20.Massaki AB, Kiripolsky MG, Detwiler SP, et al. Endoluminal laser delivery mode and wavelength effects on varicose veins in an ex vivo model. Lasers Surg Med 2013; 45:123–129.
21,Kansaku R, Sakakibara N, Amano A, et al. Histological difference between pulsed wave laser and continuous wave laser in endovenous laser ablation. Phlebology 2015; 30:429–434.
22,Proebstle TM, Moehler T, Gul D, et al. Endovenous treatment of the great saphenous vein using a 1,320nm Nd:YAG laser causes fewer side effects than using a 940nm diode laser.Dermatol Surg 2005; 31:1678–1683. Discussion 83-84.
23,Goldman MP, Mauricio M, Rao J. Intravascular 1320-nm laser closure of the great saphenous vein: a 6-to 12-month follow-up study. Dermatol Surg 2004; 30:1380–1385.
24,Hirokawa M, Kurihara N. Comparison of bare-tip and radial fiber in endovenous laser ablation with 1470nm diode laser. Ann Vasc Dis 2014; 7:239–245.
25,Vuylsteke ME, Vandekerckhove PJ, De Bo T, et al. Use of a new endovenous laser device: results of the 1,500nm laser. Ann Vasc Surg 2010; 24:205–211.
26,Schwarz T, von Hodenberg E, Furtwangler C, et al. Endovenous laser ablation of varicose veins with the 1470-nm diode laser. J Vasc Surg 2010; 51:1474–1478
